Aatomimudeli ajalugu
Atomism
Vana-Kreeka filosoofid – atomistid (Demokritos 5. saj. eKr) olid seisukohal, et kõik kehad koosnevad jagamatutest koostisosakestest – aatomitest. Atomistide käsitluses oli aatomeid 5 liiki: tuli, vesi, maa, õhk, eeter. 19. sajandi alguseks oli siiski teada, et erinevaid aatomeid on kokku umbes 100 erinevat liiki.
Tänapäevase atomistliku printsiibi kohaselt ei saa ainet (kehi) lõputult väiksemateks osadeks jagada nii, et saadud osadel säiliksid kõik jagatava terviku omadused.
Meid ümbritsevad kehad koosnevad ainetest, mille väikseimaks koostisosakeseks on molekul. Molekule on võimalik jagada omakorda teineteisega sarnaseks aatomiteks (kokku ca 120+ erinevat).
Aatomid omakorda koosnevad tuumast ja elektronkattest.
Tuuma moodustavad omavahel vastastikmõjus olevad prootonid ja neutronid, elektronkatte aga elektronid.
Kogu kaasaegne katseliselt kontrollitud osakeste füüsika lähtub Osakeste Standardmudelist, mille kohaselt aine koosneb kaheteistkümnest fundamentaal- ehk alusosakesest: kuuest leptonist ja kuuest kvargist. Need ongi aine füüsikalised algosaksesed tänapäevases tähenduses.
Daltoni piljardipallimudel
Esimese tänapäeva mõistes tõsisemalt võetava katse kirjeldada aatomit tegi John Dalton 1803. a
 Daltoni mudeli kohaselt olid aatomid homogeensed ja kerakujulised (läbimõõduga ca 100 pm) nagu piljardipallid. Kõik lihtaine aatomid olid kõik ära vahetamiseni ühesugused. Liitainete aatomid aga koosnevad erinevate elementide aatomitest.
Daltoni mudeli kohaselt olid aatomid homogeensed ja kerakujulised (läbimõõduga ca 100 pm) nagu piljardipallid. Kõik lihtaine aatomid olid kõik ära vahetamiseni ühesugused. Liitainete aatomid aga koosnevad erinevate elementide aatomitest.
Daltoni teooria kohaselt keemiliste reaktsioonide käigus aatomid ei muutu, nad paiknevad reaktsioonide käigus teineteise suhtes ümber, ainekoguse mass tervikuna aga ei muutu.
Thomsoni rosinasaiamudel

1870-del aastatel avastati katoodkiired – negatiivse elektrilaenguga “kiired”, mis tekivad vaakumisse asetatud metallitükil, mis on ühendatud vooluallika negatiivse poolusega. 1896 aastal avastas inglise füüsik Joseph John Thomson, et katoodkiired koosnevad väikestes negatiivse laenguga osakestest, mida ta hakkas nimetama elektronideks (Nobeli preemia 1906).
Thomsoni oletuse kohaselt pärinesid tema poolt avastatud elektronid aatomitest – järelikult ei saa aatomid olla homogeensed.
Nii kirjeldas Thomson aatomit kui rosinasaia (tuntud ka ploomipudingi mudelina).
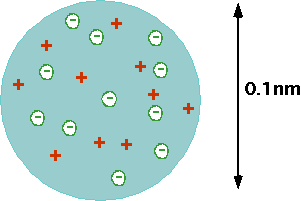
Selle kohaselt on aatomid on kerakujulised (läbimõõduga ca 100 pm) ning täidetud positiivse elektrilaengu massiga (nagu saias küpsetatud tainas), millesse on pikitud negatiivselt laetud osakesi – elektrone (nagu rosinad saias), mis saavad teatud tingimustel aatomist lahkuda – saavad tekkida katoodkiired.
Rutherfordi õhupallimudel

Uus-Meremaa päritoluga Briti füüsik Ernest Rutherford, keda tema kaasaegsed pidasid parimaks eksperimenteerijaks pärast Michael Faraday aega, püüdis 1909. aastal kontrollida Thomsoni aatomimudeli paikapidavust. Tema hüpotees oli: pommitades ainet “raskete” positiivsete alfa-osakestega (heeliumi aatomi tuumadega), peaks enamik osakestest jääma ainesse kinni ja selle tulemusena peaks aine laaduma positiivselt
Rutherford pommitaski (vt videot) väga õhukest kuldlehte alfaosakestega ning tõdes, et (1) enamik nendest osakestest läks sellest (peaaegu) suunda muutmata läbi, (2) mingi hulk osakesi põrkas aga lehelt tagasi.
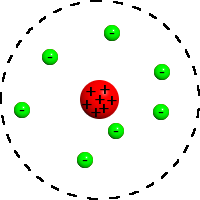
Katse tulemusena esitas Rutherford uue niinimetatud õhupallimudeli, mille kohaselt: (1) enamus aatomist läbimõõduga 100pm on tühi, (2) aatomi keskel asub väike (umbes aatomi mõõtudest 10 tuhat korda väiksem) massiivne tuum, millesse on koondunud positiivne elektrilaeng, (3) tuuma mass on ligikaudu võrdne aatomi kogumassiga ning (4) elektronid “hõljuvad” tuumalähedases ruumis nagu õhupallid.
Bohr’i planetaarmudel

Taani füüsikut Niels Bohr’i häiris Rutherfordi elektronide “õhupallikäsitlus” – negatiivse laenguga elektronid peaksid langema tuumale, mille tulemusena aatom häviks.
Võrrelnud massijaotust aatomis massi jaotumisega Päikesesüsteemis, täiendas Bohr Rutherfordi mudelit, pannes elektronid tiirlema ümber tuuma nagu tiirlevad planeedid ümber Päikese – sündis Rutherfordi-Bohr’i planetaarmudel.

On teada, et kiirendusega liikuv elektrilaeng, aga ringjoonel liikuv elektron täidab seda tingimust, peab kiirgama elektromagnetlaineid – näiteks valgust. Enamik aatomeid enamuse ajast valgust ei kiirga.
Kuna tollaste teadmistega polnud võimalik kujunenud vastuolu lahendada, sõnastas Bohr empiirilised (vaatlusandmetel tuginevad) postulaadid, mille kohaselt:
- võivad elektronid tiirelda vaid tuumast kindlatel kaugustel asuvatel orbiitidel, millest igaühele vastab kindel energia. Sellistel statsionaarsetel orbiitidel liikuvad elektronid elektromagnetlaineid ei kiirga.
- kiirgab aatom valgust (elektromagnetlaine kvandi – footoni) kui elektron temas läheb suurema energiaga orbiidilt madalama energiaga orbiidile, kui elektron läheb madalama energiaga orbiidilt kõrgema energiaga orbiidile, toimub valguse (osakese – footoni) neeldumine.
Kvantmehaanika
Osakeste leiulained
Bohr’i aatomi planetaarmudel võimaldas küll selgitada miks aatomid ei kiirga elektromagnetlaineid või kui suur on ühel või teisel orbiidil elektroni energia, kuid ta ei anna vastust küsimusele miks just need orbiidid on lubatud ja teised mitte.
1924. aastal esitles prantsuse füüsik Louis de Broglie käsitlusviisi, mille kohaselt saab kõigi aineliste liikuvate objektidega siduda teatavat liiki laine – leiulaine (ka tõenäosuslaine, mateerialaine), mille lainepikkus on pöördvõrdeline selle keha liikumishulgaga:
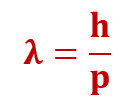
kus λ – mateerialaine lainepikkus, h = 6,62∙10-34Js – Plancki konstant ja p =mv – keha liikumishulk (kus m – keha mass, v – keha kiirus)
Seega laienes valguse korpuskulaar-laineline dualism kõikidele liikuvatele objektidele.
Miks ei me märka igapäeva elus meist mööduvaid kehi „lainetamas“?
Pole keeruline välja arvutada, et 70kg massiga inimese, kes liigub jalakäija kiirusega (6 km/h ≈ 1,7 m/s) leiulaine lainepikkus on umbes 5,6∙10-36m.
Siinkohal on paslik meenutada, et inimkonna sisemine nähtavushorisont jääb käesoleval ajal suurusjärku 10-21m – seega on inimese leiulaine lainepikkus 1015 – see tähendab umbes sama palju väiksem kui aatomituum inimesest – väiksem kui füüsikute käsutuses olevad seadmed mõõta võimaldavad.
Elektronide difraktsioon
Milline on leiulaine lainepikkus aga juhul, kui liikuvaks kehaks on elektron, mille mass on 9,1×10-31kg ning mis liigub kiirusega 10 000 km/s (energia umbes 300 eV)?
Arvutused näitavad, et sellise elektroni leiulaine pikkus on umbes 70pm.
Võrdluseks olgu meelde tuletatud, et nähtava valguse lainepikkus jäi vahemikku 380 … 760pm – ehk tegu on ultravioletsesse piirkonda jäävale elektromagnetlainele vastava lainepikkusega, mis on kaasaja vahenditega täiesti mõõdetav.
1927. aastal avastatigi elektrone, mis on ainelise mateeria ühed väiksemad koostisosakesed – st neil on kõik osakesele iseloomulikud omadused: mass, kuju, ruumala, läbi kitsaste pilude juhtides, et elektronid käituvad läbi mitme kitsa pilu minekul lainena (vt animatsiooni).
Seda nähtust nimetatakse elektronide difraktsiooniks.
Kui elektronide teele asetada vaid üksik kitsas pilu, samuti enamikus teistes olukordades, käituvad nad aga kui osakesed.
Määramatusseos
Analüüsides de Broglie’ korpuskulaar-lainelist dualismi, jõudis saksa füüsik Werner Heisenberg 1927. aastal järeldusele, et ühegi liikuva keha asukohta ja liikumishulka (sisuliselt kiirust) ei ole võimalik samaaegselt määrata kuitahes täpselt, vaid nende samaaegsel mõõtmisel kehtib määramatus:
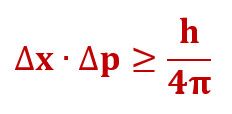
kus ∆x – keha asukoha määramatus; ∆p=m∆v+v∆m – keha liikumishulga määramatus (m – keha mass, Δm – massi määramatus, v – keha kiirus, Δv – kiiruse määramatus), h = 6,62∙10-34Js – Plancki konstant.
Kirjeldatud põhimõte pole kooskõlas meie igapäevase kogemusega – mõõdavad ju politseinikud autode kiirust ja asukohta samaaegselt ning teevad kiiruse ületajatele protokolle?
Leiame auto massiga 1000±1 kg (suhteline määramatus 0,1%) ning liigub kiirusega 100±1 km/h (suhteline määramatus 1%) asukoha määramatuse. Auto liikumishulgaks saame ligikaudu 28 000±300 kgms-1 (suhteline määramatus 1,1%) – seega asukoha määramatus
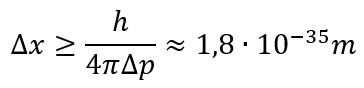
mis on taas palju-palju väiksem kui inimkonna sisemine nähtavushorisont.
Kui aga liikuvaks objektiks oleks elektron, mille mõõtmeteks hinnatakse umbes 10-18m ning mille mass on 9,1×10-31kg ja liigub kiirusega 10 000 km/s (energia umbes 300 eV)? Eeldame, et elektroni kiiruse ja massi mõõtmisel on suhteline mõõtemääramatus autoga samas suurusjärgus. Seega tuleb elektroni liikumishulga määramatus 2,8∙10-26kgms-1 ning asukoha määramatus

Määramatus tundub olevat samuti tühine? Tõdeme siiski, et elektroni asukoha määrmatus on umbes 109 korda elektroni mõõtmetest suurem!
Kui teisendame selle määramatuse autoga (mõõtmed 5m) võrreldavatesse mastaapidesse, saaksime elektroni (mis on kasvanud autoga samasse mõõtu) asukoha mõõtemääramatuseks umbes 5∙109m = 5 000 000 km ehk ringjoon, mis tähistaks (auto mõõtu) elektroni asukohta ulatuks umbes 13 korda nii kaugele kui asub Maast Kuu. Püüa siis sellisele täpsusega asukohaga mõõdetud autole teha trahvi kiiruse ületamise eest 🙂
Schrödingeri võrrand. Kvantmehaanika
 Üldistades de Broglie leiulainest ning Heisenbergi määramatusseosest tulenevaid järeldusi üldistas Saksa füüsik Erwin Schrödinger võrrandiks nn Schrödingeri võrrandiks, mis on analoogiks klassikalisest mehaanikast tuttavale liikumisvõrrandile ning kirjeldab mikromaailma objektide – aatomite, molekulide, aga ka nendes sisalduvate prootonite, neutronite ja elektronide liikumisolekuid.
Üldistades de Broglie leiulainest ning Heisenbergi määramatusseosest tulenevaid järeldusi üldistas Saksa füüsik Erwin Schrödinger võrrandiks nn Schrödingeri võrrandiks, mis on analoogiks klassikalisest mehaanikast tuttavale liikumisvõrrandile ning kirjeldab mikromaailma objektide – aatomite, molekulide, aga ka nendes sisalduvate prootonite, neutronite ja elektronide liikumisolekuid.
Schrödingeri võrrandi peamine erinevus meile tuttavast liikumisvõrrandist on see, et tema lahendiks pole mitte osakese asukoht või kiirus või kiirendus mingil ajahetkel vaid hoopis osakese leiulaine lainefunktsioon suvalisel ajahetkel.
Stephen Hawking kirjutab oma viimaseks jäänud raamatus “Lühikesed vastused suurtele küsimustele” lainefunktsiooni kohta järgmiselt: “Lainefunktsioon koosneb mistahes ruumipunkte kirjeldavatest arvudest. Lainefunktsiooni suurus näitab kui suure tõenäosusega on osakest võimalik sellest ruumipunktist leida. Suurus, millega lainefunktsioon punktist punkti varieerub, näitab ära osakese kiiruse. Lainefunktsioon võib esineda väga tugeva tõusuna väikeses piirkonnas. See tähendab, et asukoha määramatus on väike (osake asub väga suure tõenäosusga just selles ruumiosas). Samas just selles piirkonnas varieerub lainefunktsioon tugevalt. Ühel küljel üles, teisel alla – mistõttu osakese kiiruse määramatus selles piirkonnas on väga suur (on üsnagi ebaselge millise kiirusega osake selles piirkonnas liigub). Samaoodi võib esineda lainefunktsioone, kus kiiruse määramatus on väike, aga asukoha määramatus suur. Lainefunktsioon sisaldab kogu infot mida (liikuva) osakese kohta teada on. Kui on teada lainefunktsioon mingil ajahetkel, saab selle väärtused muudel ajahetkedel leida Schrödingeri võrrandi abil.”
Füüsika haru, mis kasutab osakeste asukoha ja liikumise kirjeldamisel Schrödingeri võrrandit nimetataksegi kvantmehaanikaks.
Olgu siinkohal lihtsalt ettekujutuse saamiseks toodud Schrödingeri võrrandi üldkuju:
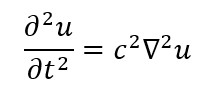
kus u ongi otsitav lainefunktsioon.
Nüüdisaegne aatomimudel
Niisiis, proovime nüüd, kus me omame arusaama elektronide lainelistest omadustest, uuesti mudeldada aatomit. On selge, et me ei saa rääkida elektronist aatomis kui kindla kuju ja mõõtmetega objektist – järelikult ei saa me ka rääkida elektroni liikumisest mingit orbiiti mööda.
Osutub, et Bohr’i poolt kirjeldatud elektronide „orbiitide“ asemel, peame kirjeldama leiulaineid, mis levivad ümber aatomituuma. Tuumaga seotud elektroni leiulaine on kui seisulaine, mis saab tuuma ümbritsedes teha ainult kindla täisarvu võnkeid – mida lähemal on elektron tuumale, seda vähem võnkeid „orbiidile“ mahub.

Niisiis, kui tahta visualiseerida aatomis liikuvat elektroni, peaksime seda ette kujutama omalaadse pilvena, mille kuju sõltub elektroni ergastatuse astmest (energiast). Pilv on seda „tihedam“ (leiulaine amplituud on seda suurem), mida suurem tõenäosus meil tuumast vastaval kaugusel on elektroni leida.
Seega oleks õigem sõnapaari „elektroni orbiit“ asemel kasutada mõistet „elektroni olek“. Kuna elektroni olekul saavad olla vaid kindlad, see tähendab kvanditud väärtused, oleks veelgi täpsem nimetada seda „elektroni kvantolekuks“.
Elektroni olekut kirjeldatakse nelja kvantarvuga
(1) Peakvantarv (n) loendab elektronkihte aatomis – seetõttu saab ta omada ainult naturaalarvulisi väärtusi: n = 1, 2, 3 …. N Mida väiksem on peakvantarv, seda lähemal on elektron tuumale. Seevastu tuumast kaugemal, suuremate peakvantarvudega elektronidel, on jälle suurem leiulaine amplituud – ehk tõenäosus elektroni „tabada“ on seal suurem.
(2) Alamkvantarv (l) määrab ära mitu elektroni mingis kihis olla saab. Mida kaugemal on leiulaine tuumast, seda rohkem elektrone sinna „mahub“. Kuna alamkvantarv loendab „osakesi“, saab ka tema omada vaid naturaalarvulisi väärtusi: l = 0, 1, 2, 3 …. N-1
(3) Magnetkvantarv (m) iseloomustab ümber tuuma „liikuva“ elektroniga seotud mikrovoolu magnetvälja. Magnetkvantarv võib omada väärtusi m = 0, ±1, ±2, ±3 … l – ± tuleb kvantarvu ette sellest, et ühel ja samal nivool paiknevate elektronide magnetväli võib olla vastassuunaline.
(4) Spinni (s) kirjeldatakse sageli kui elektroni „pöörlemist“, aga kuna elektroni puhul ei saa me rääkida pöörlevast kerakesest, siis pole selline kirjeldus täpne. Siiski – nagu pöörlemine saab toimuda päri- ja vastupäeva, saab ka spinnil olla kaks vastandarvulist väärtust +½ ja –½.
Makromaailmas kehtis tõrjutusprintsiip, mis keelas ühes ja samas ruumipunktis samaaegselt olla mitmel ainelisel objektil – selleks, et asetada raamat laual kohale, kus on juba ees teine raamat, tuleb see sealt eelnevalt ära võtta.
Mikromaailmas on tõrjutusprintsiip sõnastatud kvantarvude kaudu. Elektronide kohta aatomis kõlab see järgmiselt: aatomis ei saa olla kahte sama kvantarvude komplektiga elektroni.
Kui Dmitri Mendelejev 1870. aastal kirjeldas keemiliste elementide perioodilisussüsteemi, oli see tuletatud empiiriliselt – vaatlusandmetele tuginedes. Osutub, et võttes appi kvanditud aatomi, saame põhjendada miks mingi aatom mingisse rühma kuulub.
I rida sisaldab elemente, mille peakvantarvu väärtus on n=1. Kuna sellel „kaugusel“ on ruumi maksimaalselt kahele vastandspinnidega elektronile – spinnid vastavalt +½ ja –½, siis „mahuvadki“ esimesse ritta elemendid, milles on 1 (vesinik) või 2 (heelium) elektroni.
Teise ritta kuuluvate elementide peakvantarvu väärtus n=2 – järelikult esimesele kihile „mahub“ maksimaalselt kaks elektroni, teise saab aga juba jagada kaheks alamkihiks, millest esimesele „mahub“ kaks, aga teisele juba kuus elektroni – kokku teise kihti 8 elektroni jne. Seega on teises reas elemendid, milles on 3 … 10 elektroni
Elektronide alamkihte tähistatakse ka väiketähtedega s, p, d, f ja g – nii saab elektronide paiknemist kihtides kirjeldada elektronvalemiga – arv kihi tähise ees näitab peakvantarvu ehk elektronkihtide arvu, number tähe astendajas elektronide arvu alamkihis: H à 1s1; He à 1s2; Li à 1s22s1; Be à 1s22s2, B à 1s22s2p1; jne. Kõige viimases kihis sisalduvate elektronide arv (mis määrabki ära elemendi keemilised omadused) tuleneb sellest, millisesse rühma keemiline element kuulub. I rühma kuuluvad elemendid, mille väliskihis on 1 elektron, II rühma need, milles on 2 … kuni XII rühmani, mille väliskihis on 12 elektroni. XVIII rühmas on elemendid, mille viimane elektronkiht on elektronidega täidetud, XVII rühmas on väliskihist puudu 1 elektron, XVI on puudu juba 2 jne.
Välis-ja sisefotoefekt
Välisfotoefekt
1887. aastal avastas Heinrich Hertz, et kui valgustada negatiivselt laetud tsinkplaati, hakkab plaadi laeng vähenema – plaat emiteerib (väljastab) valguskiirguse tõttu elektrilaengut. Seda nähtust hakati kutsuma väliseks fotoefektiks. Metallist lahkunud osakeste massi ja laengu mõõtmised näitasid, et tegemist on elektronidega.
Positiivselt laetud metallplaadi puhul välist fotoefekti ei registreeritud põhjusel, et ehkki valgus lööb elektrone välja ka positiivselt laetud kehast, tõmmatakse need tänu elektromagnetilistele tõmbejõududele kehasse tagasi ning keha laeng selle pärast ei muutu.
Fotoefekti kvantitatiivseid seaduspärasusi uuris Vene füüsik Aleksandr Stoletov, kes kirjeldas plaadist valgustamise tagajärjel „välja löödud“ elektronide poolt tekitavat elektrivoolu ja märkas, et:
- metallist välja löödud elektronide hulk on võrdelises seoses plaadile langeva valguse intensiivsusega.
- metallist välja löödud elektronide maksimaalne kineetiline energia suureneb valguse lainepikkuse vähenedes ja ei sõltu valgusvoo suurusest
- kui valguse sagedus on väiksem mingist antud aine jaoks kindlast piirsagedusest, siis fotoefekti ei esine
Paraku ei osanud Stoletov selgitada miks fotoefekt tekib – tegelikult ei olnud see tollal valitsenud arusaamaga valgusest kui elektromagnetlainest põhimõtteliselt võimalik.
1900. aastal püstitas Max Planck absoluutselt musta keha kiirgust uurides hüpoteesi, et kuumad kehad ei kiirga valgust mitte pidevalt, vaid üksikute portsjonite – kvantide – kaupa. Selline lähenemine võimaldas tal statistiliselt väga täpselt kirjeldada nii erineva temperatuuriga kehade poolt kiiratava valguse värvust (sõltuvust lainepikkusest) kui ka intensiivsust (kiiratava valguse energiat).
Planck näitas teoreetiliselt, et ühe sellise energiaportsu – kvandi energia sõltub ainult kiiratava valguse sagedusest:

kus E – kvandi energia; f – kiiratava valguse sagedus ning h=6,6261∙10-34 Js – Plancki konstant, mis seob omavahel kvandi sageduse ja energia.
Kvandi energiat saab kirjeldada ka valguslaine lainepikkuse kaudu:
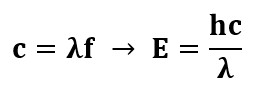
kus c=3∙108 m/s – valguse kiirus vaakumis ja λ – valguse lainepikkus.
Valguse kvante hakati kutsuma footoniteks. Paraku ei suutnud Planck esitada ühtegi tõendit kvantide reaalse olemasolu kohta.

Fotoefekti tekkimisele andis 1905. aastal lihtsa selgituse Albert Einstein, kes kasutas fotoefekti tekkepõhjuse selgitamiseks Plancki kvanthüpoteesi. Selle kohaselt tuleb elektroni ainest välja löömiseks kulutada energiat so tuleb teha tööd – niinimetatud väljumistööd.
Kui metallile langeva kvandi energia on sellest väljumistööst väiksem, siis valguse toimel elektrone välja ei lööda ning fotoefekti ei teki. Kui kvandi energia on väljumistööga võrdne, lüüakse elektron metallist välja, kuid tema „ära toimetamiseks“ on tarvis elektrivälja jõudude poolt tehtavat tööd. Kui kvandi energia on aga väljumistööst suurem, lüüakse elektron metallist välja ning väljumistööd ületav energiakogus väljendub elektroni kineetilise energiana.
Oma fotoefekti tekkimise selgituse pani Einstein kirja lihtsa võrrandina:
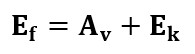
kus Ef – footoni energia; Av – elektroni väljumistöö; Ek – (välja löödud) elektroni kineetiline energia
Võttes arvesse et:
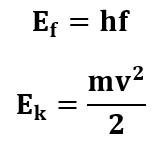
kus f – metallile langeva valguse sagedus, h=6,62∙10-34 Js – Plancki konstant; m=9.11∙10-31kg – elektroni mass; v – elektroni kiirus, saab fotoefekti võrrandile anda kuju:


Joonisel on kujutatud kaaliumiga toimuvat, kui selle pinnale langeb erinevat värvi valgus.
Kaaliumi väljumistöö on 2eV. Kui kaaliumile langeb punane valgus (lainepikkus 700 nm, energia 1,77eV), siis fotoefekti ei teki.
Rohelise valguse (550nm, 2,25eV) korral, on välja löödavate elektronide kiirus 296 km/s, violetse valguse (400 nm, 3,1eV) korral aga juba 622 km/s.
Minimaalset sagedust (või sellele vastavat maksimaalset lainepikkust), mis konkreetse aine puhul veel fotoefekti esile kutsub, nimetatakse selle aine jaoks fotoefekti punapiiriks. Punapiirile vastava kvandi energia on võrdne väljumistööga.
Sisefotoefekt
Lisaks välisele fotoefektile, kus valgus lööb ainest elektrone välja, on avastatud ka sisemine fotoefekt – valgus lööb küll aatomist elektroni välja, kuid ei väljasta elektrone ainest vaid annab neile võimaluse liikuda ainetükis teise kohta.
Sisemisel fotoefektil töötavad np-siiret omavad seadeldised – päikesepaneelid ja fotoaparaatide sensorid nn CCD (charge-coupled device) seadmed.
Aatomituuma ehitus
Tuumaosakesed
Pärast tuuma avastamist Rutherfordi poolt, käsitleti seda pikka aega homogeense tervikuna, mille mõõtmeteks hinnati ca 10-15 m
1911. aastal püstitas Hollandi füüsik Antonius van den Broek hüpoteesi, et Rutherfordi aatomituum sisaldab positiivse laenguga osakesi.
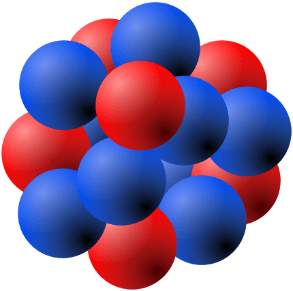
1919. aastal õnnestus Rutherfordil tõestada, et pommitades ühte ainet positiivselt laetud alfaosakestega, muunduvad ühe aine aatomid teise aine aatomiteks, kusjuures tekkivate aatomite massid erinevad teineteisest alati vesinikuaatomi tuuma täisarvkordse massi võrra – vesiniku aatomi tuuma hakati nimetama prootoniks.
Ehkki üsna pea pärast prootoni avastamist sai selgeks, et tuumas peab lisaks prootonitele olema veel teisi, ilma elektrilaenguta osakesi, avastas inglise füüsik James Chadwick osakese – neutroni, mille mass oli samas suurusjärgus prootoni massiga, kuid millel puudus elektrilaeng alles 1932. aastal.
Prootonit ja neutronit nimetatakse ka ühe nimetusega – nukleonid ehk tuumaosakesed.
Rangelt võttes peaksime ka tuumade puhul rääkima mitte kui konkreetse kuju ja mõõtmetega osakestest ja nende kogumist, vaid samuti pilvest – leiulainest, kuid piirdume käesolevas osas siiski klassikalisema variandiga ning kujutame nukleone ja nendest moodustunud tuumasid konkreetsete mõõtmetega osakestena.
Isotoobid
Keemiatunnist teame, et keemilise elemendi omadused on määratletud elektronide arvuga aatomis, veelgi täpsemalt – elektronide arvuga elektronkatte viimases kihis.
Samuti teame, et aatomid on tervikuna elektriliselt neutraalsed – see tähendab, et aatomis sisalduv positiivne laeng peab olema sama suur kui elektronide negatiivne.
Kuna prootoni positiivne elementaarlaeng on võrdne elektroni negatiivse elementaarlaenguga, saame järeldada, et aatomituumas peab olema sama palju prootoneid kui on elektronkattes elektrone.
Prootonite arvu tuumas (mis on võrdne elektronide arvuga elektronkattes) nimetatakse aatomituuma järjekorranumbriks ning seda tähistatakse tähega Z.
Neutronite arvu tuumas tähistatakse tähega N, nukleonide koguarvu tuumas nimetatakse massiarvuks ning tähistatakse tähega A. Seega on iga aatomituum (mille keemiline tähis on tinglikult X) määratud kahe täisarvuga:
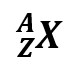
Sageli esitatakse konkreetse massiarvuga tuuma kirjeldus kujul X-A (näiteks C-12; He-4).
Sama järjekorranumbriga, kuid erineva massiarvuga tuumasid nimetatakse isotoopideks. Isotoopide keemilised omadused on identsed, kuid füüsikalised omadused on erinevad.
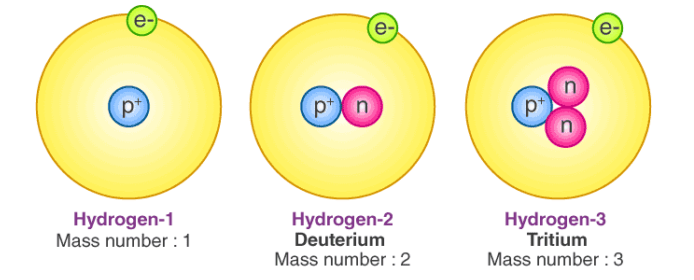
Näiteks: vesinik-1 (protium, ja vesinik-2 (deuteerium, on stabiilsed tuumad, vesinik-3 (triitium, tuumadest lagunevad aga umbes 12,3a pooled tuumadest (poolestusaeg – sellest tuleb lähemalt juttu pisut tagapool).
Samuti süsinik-12 ja süsinik-13 on stabiilsed tuumad, süsinik-11 tuumade poolestusaeg on ca 20 min, aga süsinik-14 oma 5730 aastat.
Tuumajõud
Aatomituumade koospüsimist ei ole võimalik selgitada meie poolt siiani käsitletud jõudude (gravitatsioon, elektromagnetjõud) abil.
Tuumaosakeste vahel mõjuvad teistsugust liiki jõud – tuumajõud – ja seda vastastikmõju nimetatakse tuuma ehk tugevaks vastastikmõjuks.
Nukleonide vahel mõjuvad tuumajõud on elektromagnetjõududest umbes 100 korda tugevamad. Samuti on tuumajõud on väga väikese mõjuraadiusega – nad mõjuvad ainult nende nukleonide vahel, mis asuvad teineteisest umbes 10-15 m kaugusel.
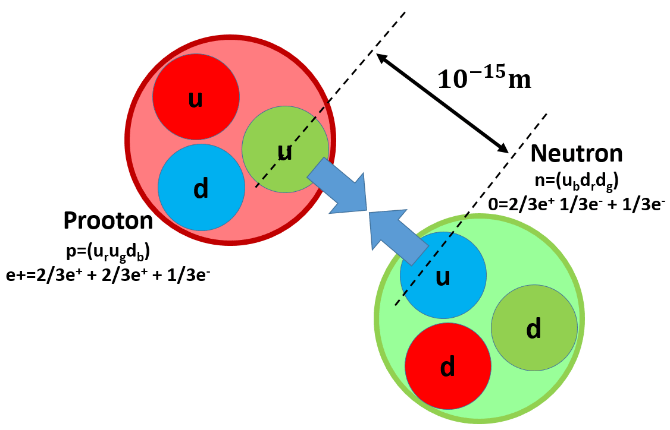
Tegelikult ei mõjugi tuumajõud mitte prootonite ja neutronite, vaid hoopis neisse igavesti vangistatud kvark-kolmikute vahel.
Kvargid on need osakesed, mille vahel mõjuvad tugeva vastastikmõju jõud. Kvargi mõjuraadius ulatub nukleonist väljapoole. Kui sellesse piirkonda satub teises nukleonis sisalduv kvark, hakkavad nad vastastikku teineteist mõjutama – nii moodustuvadki aatomituumad.
Seoseenergia. Massidefekt
Selleks, et liigutada tuumast välja seal sisalduvad nukleonid, tuleb osakestele rakendada tuumajõududega võrdseid (või nendest pisut suuremaid) jõudusid – osakeste liigutamiseks tuleb teha tööd.
Energiat, mis tuleb kulutada tuuma lõhkumiseks eraldiasuvateks nukleonideks, nimetatakse tuuma seoseenergiaks. Energiat, mis kulub tuuma lõhkumisel keskmiselt ühe nukleoni kohta, nimetatakse tuuma eriseoseenergiaks.
Massi ja energia ekvivalentsusprintsiibi kohaselt on keha energia võrdeline keha massiga:
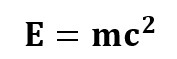
kus E – keha energia, m – keha mass ja c =3,0∙108 m/s – on absoluutkiirus.
Seega tehes tuuma lõhkumiseks tööd A ning suurendades selle arvel tuumaosakeste koguenergiat E, suurendame me kokkuvõttes nende osakeste massi:
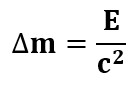
On üllatav, kuid mõõtmistega tõestatud fakt, et tuumaosakeste mass eraldi võetuna on alati suurem kui neist moodustunud tuuma mass.
Tuumade moodustumisel nendest samadest nukleonidest läheb aga massidefektiga võrdne mass „kaduma“ – järelikult peab tuumade moodustumisel prootonitest ja neutronitest vabanema seoseenergiaga võrdne kogus energiat.
Seega kui on meil on Z prootonit, mille igaühe mass on mp ja N neutronit, mille igaühe mass on mn ning nendest moodustunud aatomituum, massiga mX, siis avaldub massidefekt:
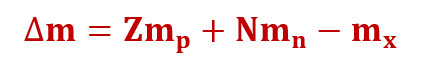
ning seoseenergia:
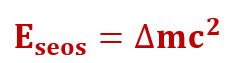
Radioaktiivsus

Radioaktiivsuse kui nähtuse avastas 1896. aastal Prantsusmaa füüsik Henri Becquerel , kes uuris uraanisoolade iseeneslikku helendamist ehk luminestsentsi (pildil on valgustamata fotoplaat, kus on näha uraanisoolade kiirguse tagajärjel tekkinud tumenemisi, mis olid analoogilised või isegi intesiivsemad valgustamisel saadutega) ning avastas, et
(1) uraanisoolad kiirgavad iseeneslikku so ilma igasuguse välismõjutuseta kiirgust;
(2) selle kiirguse intensiivsus ei sõltu aine mõjutamisest (kuumutamisest, valgustamisest, keemilistest protsessidest vms);
(3) tekkiv kiirgus on küllaltki suure läbitungimise võimega,
(4) tekkiv kiirgus ioniseerib aineid, mida ta läbib;
(5) kiirguse hulga määrab ainult uraani, mitte soola hulk preparaadis so see kiirgus on omane uraanile kui keemilisele elemendile.

Henri Becqereli poolt avastatud ainete võimet iseeneslikult kiirguda, nimetatakse radioaktiivsuseks. Suure panuse radioaktiivsuse uurimisse andsid Pierre ja Marie Curie (fotol), kes avastasid hulgaliselt radioaktiivseid keemilisi elemente (poloonium, raadium jpt) ning uurisid nende omadusi ja mõju elusrakkudele.
Curie’d tegid kindlaks, et kõik keemilised elemendid, mille järjekorranumber on suurem kui 83 on radioaktiivsed. Radioaktiivseid isotoope omavad aga ka kõik keemilised elemendid.
Ioniseerivad kiirgused ja nende toimed
Ernest Rutherford avastas, et radioaktiivset kiirgust on magnetväljas võimalik lahutada komponentideks:
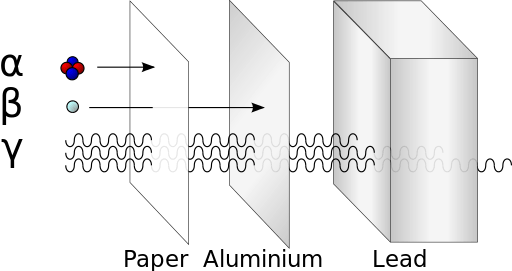
Erinevatel kiirgustel on erinev läbitungimisvõime
(1) kõige väiksema läbitungimise võimega kiirgus (teda peatab juba paberleht) hakati nimetama α-kiirguseks. Ta käitub magnetväljas nagu positiivselt laetud osakeste voog.
Tehti kindlaks, et α-kiirgus koosneb heelium-4 aatomituumadest (nimetatakse ka α-osakesteks).
(2) keskmise läbitungimisvõimega kiirgust (teda peatab 2..3 mm paksune alumiiniumleht) hakati nimetama β-kiirguseks. See käitub magnetväljas nagu negatiivselt laetud osakeste voog.
Tehti kindlaks, et β-kiirgus koosneb elektronidest (nimetatakse ka β-osakesteks).
(3) kõige suurema läbitungimisvõimega kiirgust (1cm paksune plii kiht vähendab kiirguse intensiivsust kõigest kaks korda), hakati nimetama γ-kiirguseks. Magnetväli ei avalda tema kulgemisele mingit mõju.
Selgus, et γ-kiirgus on väga väikese lainepikkusega (λ<10-11m) ja väga suure energiaga elektromagnetlaine.

Samuti käituvad erinevad kiirgused magnet- või elektrivälja sattudes erinevalt
Radioaktiivsed muundumised
Radioaktiivset kiirgust uurides tõdeti, et see kiirgus on hämmastavalt muutumatu, selle selle eraldumisega kaasneb märgatav energia eraldumine ning lõpuks, et radioaktiivset kiirgust kiirgav keemiline element muundub selle käigus teiseks elemendiks.
Inglise füüsik Frederick Soddy sõnastas niinimetatud nihkereeglid alfa- ja beetakiirguste kohta. Gammakiirgusega ei kaasne tuumalaengu muutumist.
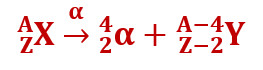
Alfa-lagunemisel kaotab tuum kahekordse elementaarlaengu suuruse positiivse elektrilaengu ning tema mass väheneb ligikaudu nelja aatommassi ühiku võrra isotoobi tuum nihkub perioodilisuse süsteemis kahe ruudu võrra ettepoole:
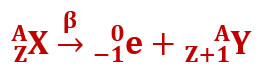
Beeta-lagunemisel lendab tuumast välja elektron, mille tõttu tuumalaeng suureneb ühe ühiku võrra, tuuma mass aga jääb samaks isotoobi tuum nihkub ühe ruudu võrra perioodilisuse süsteemi lõpu poole:
Tõepoolest, beeta-lagunemisel lendab elektron välja aatomituumast.
Nimelt võime neutronit teatud olukorras käsitleda kui prootonist ja elektronist
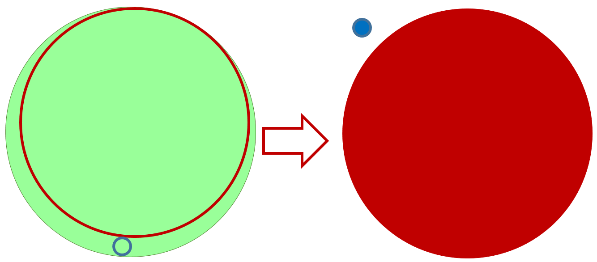
koosnevat liitosakest, mis sobivatel tingimustel laguneb prootoniks ja elektroniks. Prooton jääb tuuma, suurendades selle järjekorranumbrit, elektron aga paisatakse tuumast välja.
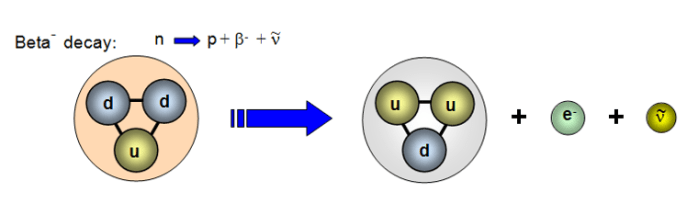
Veelgi täpsemalt selgitades muutub teatud tuumasiseste protsesside käigus üks neutronis sisalduv d-kvark u-kvargiks ning lisaks elektronile vabaneb beetalagunemise käigus veel ka elektronantineutriino.
Stabiilsed tuumad
Radioaktiivseid isotoope on oluliselt enam kui stabiilseid – seega on tuuma stabiilsus pigem erand kui reegel.
Selleks, et tuum saaks olla stabiilne peab olema täidetud kolm tingimust:
- Kuna tuuma suurus on piiratud, siis peab leiduma optimaalne osakeste arv, et tuuma seoseenergia oleks antud tingimustes minimaalsed;
- Prootonite ja neutronite energiatasemed peavad olema täidetud alates madalaimast;
- Prootonite ja neutronite energiatasemed peavad olema täidetud võrdses ulatuses
Poolestusaeg
Radioaktiivsust uurides avastati, et iga radioaktiivse isotoobi jaoks on olemas kindel aeg – poolestusaeg – mille jooksul tema kiirguse intensiivsus väheneb poole võrra. Poolestusaja vältel jõuavad ära laguneda keskmiselt pooled ainekoguses sisaldunud radioaktiivse isotoobi tuumad.
Teades isotoobi poolestusaega τ ning tuumade arvu vaatluse alghetkel N0, saame leida lagunemata radioaktiivsete osakeste arvu N aja Δt möödudes valemist – radioaktiivse lagunemise seadusest:
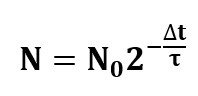
Poolestusaeg on statistiline suurus – ta ei ütle midagi konkreetse osakese eluea kohta.
Mõnede isotoopide poolestusajad: vesinik-3 (triitium) – 12,3 aastat; süsinik-14 – 5730 aastat; radoon-222 – 3,825 päeva; uraan-238 – 4,5 mld aastat; plutoonium-239 – 24 400 aastat.
Mida lühem on poolestusaeg, seda intensiivsemat kiirgust see isotoop põhjustab ning seda suuremat ohtu kujutab ta inimeste tervisele. Samas väheneb lühikese poolestusajaga isotoopidega saastatud piirkonnas radioaktiivsuse tase kiiresti ning selle taaskasutusele võtmiseks kulub oluliselt vähem aega kui pika poolestusajaga isotoopide korral.
Radioaktiivne dateerimine
Poolestusaja uurimisel põhineb orgaanilise aine radioaktiivse dateerimise meetod.
Eluslooduses toimub pidev süsinikuringe. Kõik elusorganismid tarbivad ja eritavad süsinikku. Looduslik süsinik jaguneb isotoopide vahel järgmiselt: 98,89% looduses leiduvatest isotoopidest on stabiilsed süsinik-12 ja 1,11% süsinik-13 isotoobid, ülejäänud, alla 1% looduses esinevatest süsiniku isotoopidest (C-11, C-14, C-15) on radioaktiivsed ning nende tuumade esinemissagedus on Maal ja seetõttu ka kõikides elusorganismides fikseeritud alati kindlas proportsioonis.
 Kui organism elab, siis on radioaktiivsete süsiniku isotoopide omastamine ja organismist väljutamine tasakaalus. Kui organism sureb, siis lakkab tema süsinikuvahetus – temas sisalduvad radioaktiivsed isotoobid küll lagunevad, kuid uusi radioaktiivseid isotoope ümbritsevast keskkonnast ei omistata. Süsinik-14 poolestusaeg on 5730 aastat, teistel radioaktiivsetel isotoopidel on see palju lühem. Nii võimaldab süsinik-14 isotoobi proportsiooni uurimine tuvastada mitu aastat tagasi lõppes orgaanilise aine osalemine süsinikuringes eh teisisõnu, millal uuritav süsinikukandja suri.
Kui organism elab, siis on radioaktiivsete süsiniku isotoopide omastamine ja organismist väljutamine tasakaalus. Kui organism sureb, siis lakkab tema süsinikuvahetus – temas sisalduvad radioaktiivsed isotoobid küll lagunevad, kuid uusi radioaktiivseid isotoope ümbritsevast keskkonnast ei omistata. Süsinik-14 poolestusaeg on 5730 aastat, teistel radioaktiivsetel isotoopidel on see palju lühem. Nii võimaldab süsinik-14 isotoobi proportsiooni uurimine tuvastada mitu aastat tagasi lõppes orgaanilise aine osalemine süsinikuringes eh teisisõnu, millal uuritav süsinikukandja suri.
Radioaktiivse süsiniku meetod vähem kui 1%-lise täpsusega teha kindlaks, millal uuritav objekt süsinikuringest lahkus ehk suri. Meetod ei sobi hästi mõnikümmend või mõnisada aasta aastat tagasi surnud organismide vanuse dateerimiseks, kuid kui uurime mõni tuhat või koguni mõni miljon aastat tagasi elanud organismide jäänuseid, on radioaktiivse dateerimise meetod asendamatu abivahend leitud jäänuste vanuse kindlaks tegemisel.
Kiirgusdoos
Radioaktiivse kiirguse ohtlikus organismidele oli teada peaaegu selle avastamisest alates. 20. sajandi jooksul lisandus sellele ebamäärasele ohule teadmine, et radioaktiivne kiirgus põhjustab vähki (kantserogeenne toime) ning geneetilisi mutatsioone järglastel.
Tegelikult peame selle eest, et elu Maal üldse olemas on, tõenäoliselt samuti tänama radioaktiivset kiirgust, sest tänu maapinnas leiduvate radioaktiivsete isotoopide pidevale lagunemisele, asub kogu elusloodus pidevas kiirgusvoos.
Neid kiirgusliike, mis võivad otseselt surmata rakke, muuta nende DNA-d või tekitada muid kahjustusi, nimetatakse ioniseerivateks kiirgusteks.
Ioniseeriva kiirguse koguse – kiirguse doosi – mõõtmiseks kasutatakse ühikuna greid (1Gy). Neeldunud kiirgusdoos on võrdne ühe greiga, kui keha ühes kilogrammis neeldub 1 džaul kiirgusenergiat:
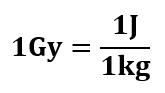
Kiirguse mõju elusorganismile kirjeldatakse ekvivalentdoosiga, mida mõõdetakse siivertites (1Sv). Ka siivert kirjeldab ühes kilogrammis elusorganismis neeldunud kiirgusenergia kogust džaulides, kuid kiirguse doosi korrigeeritakse faktoriga, mis arvestav liikide eripära ja muid üksikasju.
Kuna saadud kiirgusdoos kumuleerub – eelnevalt omandatud doosile liitub pidevalt juurde saadav doos, siis loetakse inimesele ohutuks loetakse kiirgusdoos, mis ei tohi ületada 100 mSv viie järjestikkuse aasta jooksul kumuleeruvana või 50 mSv aastas. Surmavaks loetakse ühekordset doosi 3…5 Sv, kiiritustõbi tekib ekvivalentdoosiga 1…3 Sv.
Tuumaenergia
Tuumareaktsioonid
Keemiliste reaktsioonide käigus muunduvad ühed reaktsioonist osa võtvad ained teisteks aineteks. Reaktsioonide käigus säilivad kõik reaktsioonist osa võtnud aatomid:
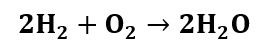
Tuumareaktsioonide käigus muunduvad ühe keemilise elemendi aatomid (tuumad) teiste elementide aatomiteks (tuumadeks), säilivad kõik reaktsioonist osa võtnud nukleonid:
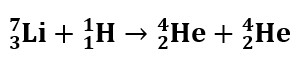
Raskete tuumade lõhustumine
Raskete tuumade lõhustumiseks ei loeta neid reaktsioone, mille käigus eralduvad ainult alfa- või beetaosakesed.

Raskete tuumade lõhustumisel lagunevad tuumad mitmeks väiksema järjekorranumbri ja massiarvuga tuumaks.
Esimese raskete tuumade iseenesliku lõhustumise avastasid 1938. aastal Saksamaa füüsikud Otto Frish ja Lise Meitner (mõnede allikate puhul nimetatakse esimesteks raksete tuumade lõhustumisreaktsioonide avastajateks Saksa füüsikuid Otto Hahni ja Fritz Strassmanni) – selle reaktsiooni käigus vabaneb 168 MeV (2,69·10-11 J) energiat ühe lagunemisakti kohta.
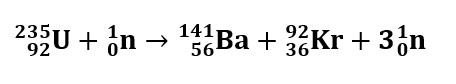
Ahelreaktsioon
Raskete tuumade lõhustumisel vabanevad neutronid võivad põhjustada järgmiste uraanituumade lõhustumist – seda nähtust nimetatakse ahelreaktsiooniks.
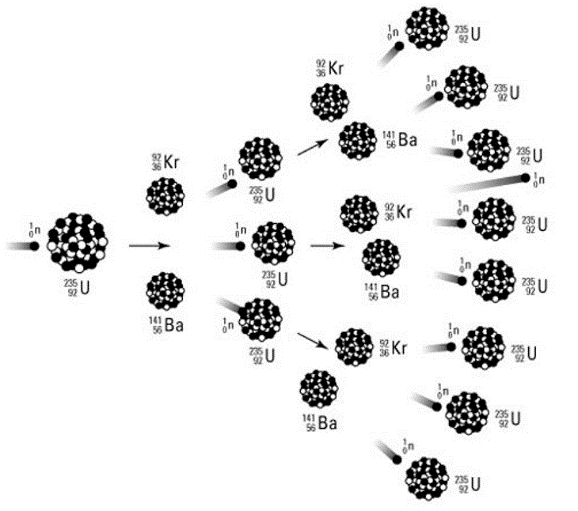
Kuna iga lõhustumisakti kohta vabaneb lisaks reaktsiooni esile kutsuvale neutronile kaks uut neutronit, suureneb ahelreaktsioonides lõhustuvate tuumade hulk geomeetrilises progressioonis.
Ahelreaktsioon saab käivituda, kui potentsiaalselt lõhustuda võivate tuumade hulk on piisav ehk ainekogus ületab teatava kriitilise väärtuse nö kriitilise massi.
Uraan-235 tuumade ahelreaktsiooni käivitamiseks peab selliste tuumade mass, eeldusel, et ainetükk on ideaalse kera kujuline ning aine puhtusaste on 100% olema võrdne või ületama 900 grammi . Plutoonium-239 tuumade jaoks on samadel tingimustel kriitiline mass umbes 0,3 kg.
Ahelreaktsiooni olemuse avab hästi juuresolev videosimulatsioon
Tuumasünteesi reaktsioonid
Ajalooliselt kõige esimene tuumareaktsioon viidi läbi 1932.a, kui pommitati liitium-6 tuumi deuteeriumi tuumadega. Tulemuseks saadi 2 alfaosakest ehk heelium-4 aatomituuma.
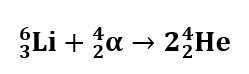
Kergete tuumade ühinemisreaktsioonide uurimise käigus avastati tehisradioaktiivsuse nähtus – see on nähtus, kus tuumade pommitamisel kergete tuumadega (H, D, He-4 jpt) tekivad radioaktiivsed isotoobid, mida looduses ei leidu.
Esimene tehislikult loodud isotoop oli fosfor-30:
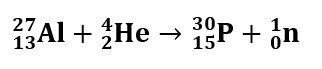
Looduslikke stabiilseid isotoope on vaid 80 elemendil – kokku ca 260 tükki (keskmiselt 3,2 stabiilset isotoopi elemendi kohta). Radioaktiivseid tehisisotoope on tänaseks avastatud juba üle kaugelt üle 3000
Tuumareaktsioonid ja energia
Nii raskete tuumade lõhustumisreaktsioone (fissiooni) kui ka kergete tuumade sünteesireaktsioone (fusiooni) ühendab asjaolu, et nendes vabaneb energiat, sest
- reaktsiooni lähtetuumade seoseenergia on alati suurem kui tekkivatel tuumadel ehk
- tuumareaktsioonide lähtetuumade seisumass tekkivate tuumade omast suurem või
- tuumareaktsioonides muundub alati teatav osa massist energiaks.
Nende kolme asjaolu puhul on tegemist ühe ja sama nähtuse erineva vaatenurgaga.
Tuumarelv
1933.a ennustas Ungari teadlane Leó Szilárd ahelreaktsiooni tekkimise võimalust ning ja patenteeris selle kasutamise idee tuumapommis ja tuumareaktoris. Detsembris 1938 avastavad saksa keemikud Otto Hahn ja Fritz Strassmann esimese uraanituuma iseenesliku lõhustumise baariumiks ja krüptooniks (O. Frisch ja L. Meitner jõuavad samale tulemusele 1939.a jaanuaris ja esitavad täpsema teooria).
1939.a käivitab USA valitsus nn Manhattani projekti eesmärgiga valmistada tuumaenergial töötav pomm. 2. detsember 1942 – kutsutakse Chicago ülikoolis valminud tuumareaktoris Enrico Fermi juhtimisel esile esimene ahelreaktsioon.
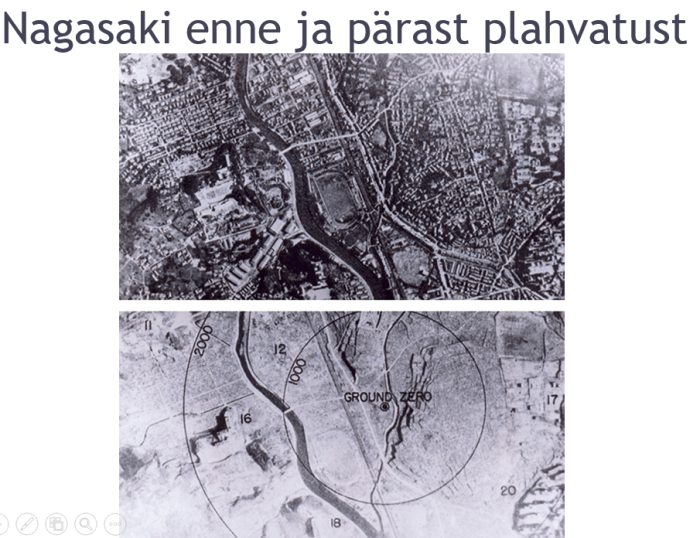
16. juuli 1945 viiakse USA-s Los Alamose kõrbes läbi esimene tuumapommi katsetus – Project Trinity, kus õhiti lõhkeseadeldis nimega The Gadget. Esimest korda kasutati tuumapomme lahingtegevuses 6. augustil 1945. aastal Hiroshimas, kui linnale heideti uraanipomm koondnimega Little Boy, teist ja viimast korda “lahingtegevuses” 9. augustil 1945. aastal Nagasakis, kus linnale heideti plutooniumipomm koondnimetusega Fat Man.
 |
|
| Little Boy (koopia-mudel esiplaanil) | Fat Man (koopia-mudel tagaplaanil) |
| Mass 4400 kg, Pikkus 3m, Läbimõõt 0,71mPlahvatusvõimsus 16 kilotonni (st 16 000 tonni tavalõhkeaine plahvatuse ekvivalendis)
Tuumakütust U-235 ca 64 kg, millest reageeris ca 50 kg ning ca 0,6g ainet muundus energiaks Hukkunuid: ca 66 000 plahvatuse hetkel + ca 69 000 mõne päeva jooksul peale plahvatust erinevatesse vigastustesse +vähemalt 200 000 surnut erinevatesse kiiritusega seotud haigustesse järgmise 5 aasta jooksul |
Mass 4 633 kg, Pikkus 3,3m, Läbimõõt 1,5mPlahvatusvõimsus 21 kilotonni (st 21 000 tonni tavalõhkeaine plahvatuse ekvivalendis)
Tuumakütus Pu-239 ca 6,2kg, millest jõudis reageerida 17% ning energiaks muundus ca 1g ainet Hukkunuid: ca 40 000 plahvatuse hetkel + ca 40 000 mõne päeva jooksul peale plahvatust erinevatesse vigastustesse + vähemalt 100 000 surnut erinevatesse kiiritusega seotud haigustesse järgmise 5 aasta jooksul |
 |
 |
 |
|
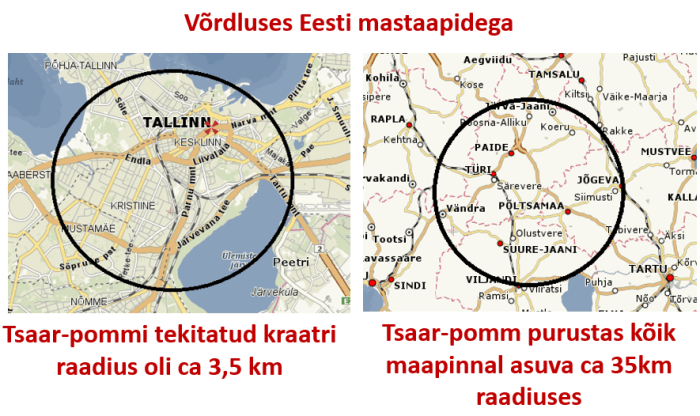
| Tsaar-pommMass 27 000 kg, Pikkus 8 m, Läbimõõt 2,1 m
Plahvatusvõimsus 57 megatonni – st 57 milj. t tavalõhkeaine ekvivalendis so 1 140 000 raudteevagunitäit a 50 tonni. Tuumakütus (tõenäoliselt): 50% plahvatuse energiast saadi U-235 lõhustumisest ja 50% energiast vesinikupommi plahvatusest |
|
 |
|
Dokumentaalkaadrid Tsaar-pommi plahvatusest
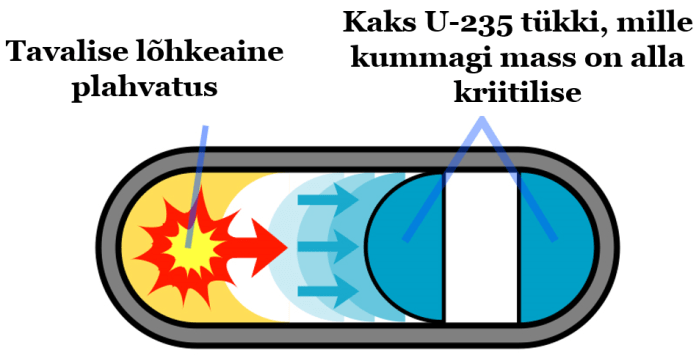
Tuumapommi plahvatama panemiseks kutsutakse esile U-235 (või Pu-239) ahelreaktsioon, seega peab pommis sisalduva “tuumalõhkeaine” mass olema suurem kriitilisest massist. Ahelreaktsioon vältimiseks soovimatul hetkel peab transportimise ajal olema “tuumalõhkeaine” mass kriitilisest väiksem ning muutuma kriitilisest massist suuremaks plahvatuse hetkel.
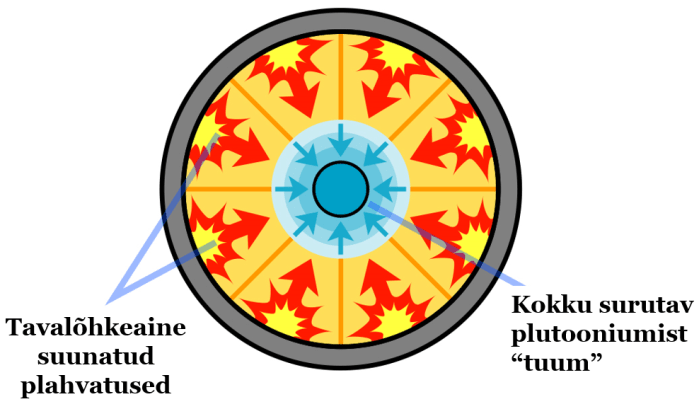
Selleks on 2 võimalust: (1) “tuumalõhkeainet” transporditakse kahes tükis, mis plahvatushetkel ühendatakse niinimetatud kahuritorumeetod (joonis vasakul); (2) “tuumalõhkeaine” ruumala hoitakse transportimisel kriitilisest suuremana ning plahvatuse hetkel see surutakse kokku vajalike mõõtmeteni niinimetatud kompressioonimeetod (joonis paremal).
 |
 |
Ajaloo kõige suurema tuumapommi “Tsaar-pommi”, võimsusega 57 megatonni õhkis Nõukogude Liit 30. oktoobril 1961. aastal Novaja Zemlja saarestikus (vt videost plahvatust). Kokku on maailmas aastatel 1945 … 1998 tehtud üle 2000 tuumakatsetuse – USA – 1054 katsetust, Nõukogude Liit – 715, Prantsusmaa – 210, Suurbritannia – 45, Hiina – 45, India – 6 ning Pakistan – 6. Tuumakatsetusi on tehtud ja tuumarelv on ka Iisraelil, Lõuna-Aafrika vabariigil, Põhja-Koreal – aga vastavad väited on riikide poolt kinnitamata.
Viimane (ametlik) tuumakatsetus toimus: Nõukogude Liidus 1990, Suurbritannias 1991, USAs 1992, Prantsusmaal, Hiinas 1996 ja Põhja-Koreas septembris 2016.
10. septembril 1996.a kirjutati ÜRO-s alla tuumakatsetuste täieliku keelustamise lepe (Comprehensive Nuclear-Test-Ban Treaty ehk CTBT), seda moratooriumit on rikkunud vaid Põhja-Korea, India ja Pakistan.
Tuumareaktor
Tuumareaktoris toimub juhitud ahelreaktsioon ning hoitakse ära selle kasvamine plahvatuseks. Esimene tuumareaktor käivitati 1942. aasta lõpus Chicago ülikoolis (USA). Esimene tsiviilkasutuses energia tootmise tuumareaktor – AM-1 (“Атом Мирный” vene keeles „rahumeelne aatom“) – käivitati 1954. aastal Moskva lähistel (Venemaa).
 Tuumareaktori tähtsaimaks osaks on tuumakütus, mida hoitakse eriliste varrastena – igaühe mass väiksem kriitilisest, varraste mass reaktori piirkonnas kokku ületab aga kriitilise massi.
Tuumareaktori tähtsaimaks osaks on tuumakütus, mida hoitakse eriliste varrastena – igaühe mass väiksem kriitilisest, varraste mass reaktori piirkonnas kokku ületab aga kriitilise massi.
Reaktsiooni “rahulikuks” toimumiseks hoitakse ahelreaktsiooni käigus tekkivate neutronite arv kontrolli all eriliste juhtvarrastega, mis on valminud neutroneid neelavast materjalist ning aeglustist, et reaktoris tekkivad neutronid liiguksid sobiva kiirusega (liiga kiiresti liikuvad neutronid põrkuvad U-235 tuumadega ega lõhusta neid). Reaktoris vabanev seoseenergia, mis muundub peamisel soojusenergiaks, juhitakse reaktori töötsoonist välja spetsiaalse vedeliksärgi abil.

Tuumareaktoreid kasutatakse peamiselt elektrijaamades (fotol Olkiluoto jaam Soomes Rauma linna lähedal), aga ka laevadel elektri tootmiseks.

Tuumaenergia senisest laialdasema kasutusele võtmise kasuks räägib jaamade suur väljundvõimsus ning asjaolu, et tuumakütuse varud on väga-väga suured. Ära ei saa jätta märkimata ka seda, et tuumajaamad ei tekita elektrienergia tootmisel kasvuhoonegaase.

Selle vastu räägivad aga tuumajäätmete utiliseerimise keerukus, uraani tootmisega seonduvad keskkonnaprobleemid ja ohud inimestele ning inimeste tohutu eelarvamus tuumaenergia suhtes, et „mis siis kui midagi läheb valesti“. Kartus võib olla põhjendatud, sest tuumajaamas toimuval õnnetusel on ülisuur kahjulik mõju väga pikaks ajaks küllalt suurele jaama ümbritsevale piirkonnale (fotol Tšornobõli tuumaelektrijaama IV plokk pärast seal toimunud plahvatust – tegu on inimkonna suurima tuumakatastroofiga Hiroshimale ja Nagasakile heidetud tuumapommide järel).
Kahtlemata ongi üheks tuumaenergia laialdasema kasutusele võtmise takistuseks ka võimalus, et tuumareaktorites tekkivatest jäätmetest valmistatakse tuumapomm või kasutatakse neid muul viisil massihävitusrelvana.
Tuumajaama suurõnnetus Fukushimas
Termotuumarelv
Termotuumarelvaks ehk vesinikupommiks nimetatakse seadeldist, mis saab oma energia kergete tuumade sünteesireaktsioonis vabanevast seoseenergiast.

Termotuumareaktsioonide käivitamiseks on tarvis: (1) termotuumakütust (raske- (D) ja üliraske (T) vesiniku segu või liitiumdeuteriid) ning (2) väga kõrget temperatuuri, mis reaktsiooni käivitab.

Termotuumapommi tööpõhimõte: (1) esmalt pannakse plahvatama väike tuumapomm, millega luuakse piisavalt kõrge temperatuur, (2) seejärel toimub termotuumakütuse “plahvatus”
Termotuumapommi plahvatuses vabanev energia on palju suurem kui tuumapommil. 1 kg termotuumakütuse reageerimisel vabanev energia on võrdne ca 65 miljoni tonni tavalõhkeaine plahvatusel vabaneva energiaga (65 MTNT)
Esimene termotuumapomm – “Ivy Mike” (vt videot) – õhiti 1952. aastal USA-s.
Termotuumareaktor
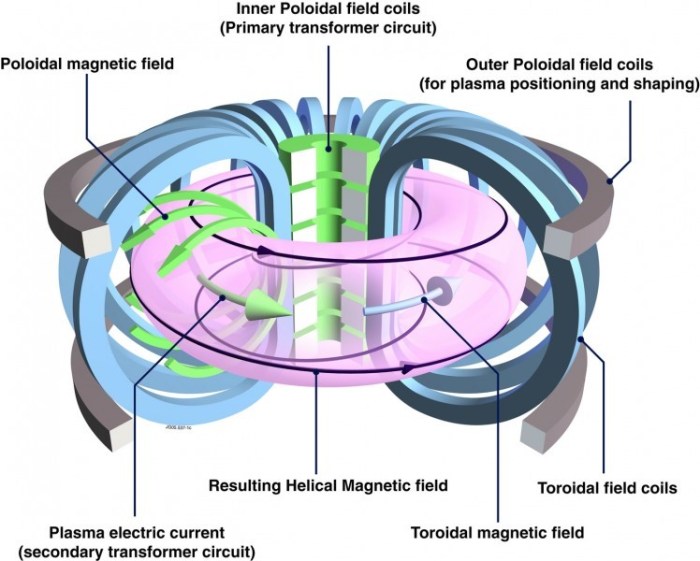
Termotuumareaktsioonide käivitumise tingimuseks on aineosakeste ülikõrge temperatuur – TOKAMAK-seadeldises ehk termotuumareaktoris (“тороидальная камера с магнитными катушками” – magnetpoolidega toroidkamber) on temperatuur umbes 100 mln kraadi. Sellisel temperatuuril on aine täielikult ioniseeritud olekus (plasma) ning tema olek on äärmiselt ebastabiilne.
TOKAMAK-seadeldises olev plasma, mis on ümbritsetud peaaegu täieliku vaakumiga ning „vangistatud“ ülitugevasse magnetvälja – tänu sellele garanteeritakse, et plasma ei puutu kokku reaktori osadega, sest mis tahes materjal aurustuks/sublimeeriks nii kõrge temperatuuriga kehaga kokku puutudes silmapilkselt.
Termotuumareaktori kütuseks on deuteeriumi- ja triitiumi (raske ja üliraske vesinik) segu. Paraku peame tunnistame, et vaatamata oma perspektiivsusele ja tohutule energiale, mis sünteesireaktsioonides eraldub, kulub plasma stabiilsena hoidmiseks ja vajaliku temperatuurini kuumutamiseks veel rohkem energiat, kui reaktsioonides vabaneb.
You must be logged in to post a comment.